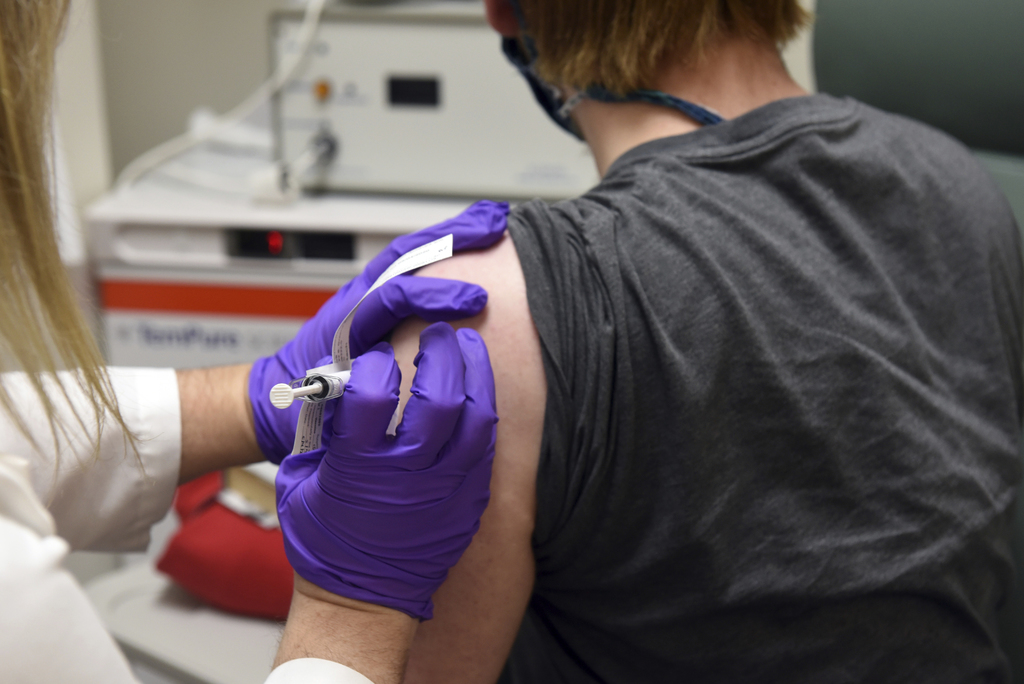
La vacuna BNT162b2, basada en tecnología de ARN mensajero, está siendo desarrollada conjuntamente con la alemana BioNTech. (AP)
La farmacéutica estadounidense Pfizer anunció este lunes que su vacuna contra la COVID-19 es eficaz en un 90 %, por encima de lo requerido por los reguladores estadounidenses, lo que permite augurar una rápida autorización de emergencia para su puesta a disposición del público, algo que podría suceder antes de final de este año.
"Hemos encontrado que la vacuna es más del 90 % efectiva en la prevención de la COVID-19 en participantes sin evidencias previas de infección del SARS-CoV-2 en los primeros análisis interinos", indicó en un comunicado la farmacéutica, que es la primera empresa occidental en presentar datos de eficacia de la vacuna necesarios para su distribución.
Este es el gran hito que la Administración del presidente Donald Trump llevaba esperando desde que lanzó la llamada Operación "Warp Speed" (velocidad de la luz), un programa multimillonario para desarrollar en tiempo récord con el sector privado vacunas y terapias contra la COVID-19, que ha asolado EUA, está fuera de control y ha dejado ya más de 237, 000 muertes en este país.
La vacuna BNT162b2, basada en tecnología de ARN mensajero, está siendo desarrollada conjuntamente con la alemana BionNTech y ha pasado por un riguroso proceso de ensayos clínicos y un análisis de los datos preliminares de la fase 3 por parte de un comité independiente y externo que ha determinado su eficacia.
"Hoy es un gran día para la ciencia y para la humanidad. Los primeros resultados de nuestra Fase 3 de las pruebas de la vacuna de COVID-19 proveen evidencia inicial de la habilidad de nuestra vacuna de prevenir la enfermedad", indicó en un comunicado Alberto Bourla, consejero delegado de Pfizer.
El alto nivel de eficacia se ha logrado siete días después de la segunda dosis, es decir 28 días después del inicio de la vacunación, que requiere dos inyecciones, aunque Pfizer y BioNTech advierten que la eficacia final podría variar a medida que avancen los estudios.
Pfizer detalló que esperan tener dos meses de datos de seguridad acumulados en la tercera semana de este mes de noviembre, con lo que podrían así satisfacer los requisitos de la Agencia de Alimentos y Medicamentos de EUA (FDA, en sus siglas en inglés) para pedir la autorización de emergencia.
Una vez obtenida, la vacuna podrá ser distribuida y administrada, algo para lo que las autoridades estadounidenses han preparado planes que darán prioridad al personal sanitario, empleados esenciales, poblaciones de riesgo y a zonas con mayor ritmo de infección.
"Basados en nuestras proyecciones, esperamos producir globalmente hasta 50 millones de dosis de la vacuna en 2020 y hasta 1, 300 millones de dosis en 2021", señaló Pfizer en su comunicado.
BIDEN Y TRUMP REACCIONAN
Pese a que Trump había puesto muchas esperanzas de reelección en presentar una vacuna antes de los comicios del 3 de noviembre, los datos clínicos han llegado dos días después de que se confirmara su derrota y que su rival, el demócrata Joe Biden, será su sucesor en enero.
Biden, que ha creado un grupo de trabajo para controlar la pandemia, se apresuró hoy a reconocer este avance que es, es su opinión, "causa para la esperanza", pero no es "el final de la batalla contra la COVID-19".
Por su parte el presidente Trump criticó este lunes a Pfizer y a la Administración de Medicamentos y Alimentos (FDA), por no haber anunciado antes los resultados de la vacuna de la farmacéutica.
"La FDA y los demócratas no querían que lograse un triunfo en vacunas antes de las elecciones, así que ha salido cinco días después, ¡Como dije todo el tiempo!", dijo en una serie de tuits Trump.
BRASIL SUPENDE TEMPORALMENTE ENSAYOS DE LA VACUNA
La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil determinó la suspensión temporal de los ensayos clínicos en el país de la vacuna contra el coronavirus desarrollada por el laboratorio chino Sinovac, tras ser notificada de la ocurrencia de un “evento adverso grave”.
Anvisa “decidió interrumpir el estudio para evaluar los datos observados hasta el momento y juzgar sobre el riesgo/beneficio de la continuidad del estudio” después de que fuera notificada sobre un evento adverso grave el pasado 29 de octubre.
“Esta clase de interrupción es prevista por las normativas de Anvisa y hace parte de los procedimientos de Buenas Prácticas Clínicas, esperado para estudios clínicos conducidos en Brasil”, precisó la entidad en un comunicado.
Con la interrupción de las pruebas clínicas, que incluyen a 9, 000 voluntarios en Brasil, ningún nuevo individuo podrá ser vacunado.
Anvisa no dio a conocer más detalles sobre la suspensión de las pruebas de la Coronavac, que se está probando en la fase 3 de ensayos clínicos en Brasil, Turquía, Bangladesh e Indonesia, además de China, para respetar los “principios de confidencialidad, dignidad humana y protección de los participantes”.
El regulador no precisó cuál fue el evento grave que motivó la decisión, pero explicó que son considerados como “efecto adverso grave” los casos de muerte, evento adverso potencialmente fatal, incapacidad o invalidez persistente o significativa o internamiento hospitalario del paciente.
Anomalías congénitas o defectos de nacimiento, sospechas de transmisión de agente infeccioso por un dispositivo médico o “evento clínicamente significativo” igualmente configuran reacciones colaterales graves, agregó.